Унутрашња енергија и кретање молекула

При спремању хране електрична енергија се претвара у топлотну → топлота је само један од видова енергије.
Свако тело је систем састављен од микрочестица – молекула (најситнији делићи који још увек задржавају особине посматраног тела) и атома (саставни део молекула) који се непрестано крећу и стално међусобно сударају услед чега мењају брзину, правац и смер кретања.
Неуређено (хаотично) кретање микрочестица назива се топлотно кретање. Оно је унутрашње кретање у самим телима, а одговарајућа енергија је унутрашња енергија. Што је кретање молекула брже то је већа унутрашња енергија.

пример:
- загрејана вода има већу унутрашњу енергију од хладне воде која има већу унутрашњу енергију од леда.
- водена пара има већу унутрашњу енергију од вреле воде

Температура и топлотно ширење тела
Температура је физичка величина којом се описује степен загрејаности тела.
Она карактерише унутрашње стање тела и мери унутрашњу енергију тела.
У свакодневном животу користи се скала са степенима Целзијуса [°C], али је јединица температуре у Међународном систему јединица келвин [K].
|
t [ºC]
|
појава
|
T[К]
|
|
100
|
кључање воде
|
373
|
|
0
|
мржњење воде
|
273
|
|
−100
|
|
173
|
|
−273
|
најнижа могућа температура – апсолутна нула
|
0
|
Температура по Келвиновој скали Т се израчунава тако што се броју 273 дода температура t мерена у Целзијусовој температурној скали
Т=(273+t/ºC)K
обрнуто
t=(T/K-273)ºC
Поред ове две температурске скале користи се и Фаренхајтова и Реомирова скала.

За тачно мерење температуре служе термометри чији је принцип рада заснован на особини тела да се шире при загревању.
 Најчешће се жива или алкохол загревају у резервоару и шире се.
Најчешће се жива или алкохол загревају у резервоару и шире се.


Тела се при загревању шире, а при хлађењу сакупљају увек на исти начин.
након загревања металне лопте она не може да прође кроз прстен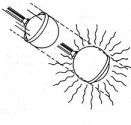
не шире се све супстанце на исти начин: посматрамо биметалну траку

Течности се при загревању више шире него чврста тела, а највише се шире гасови.


Тела се шире на топлоти, јер се молекули брже крећу, више сударају и распоређују на веће међусобно растојање па тело повећава своју запремину.
Аномалија воде
Када се вода загрева почевши од 0˚C, она најпре смањује своју запремину до 4˚C, а затим се даље шири слично осталим телима. Према томе, вода на 4˚C при нормалном атмосферском притиску има максималну густину, која је усвојена као јединица густине.
Количина топлоте
Унутрашња енергија НИЈЕ топлота. Топлота је онај део унутрашње енергије који се са тела више температуре спонтано преноси на тело ниже температуре.
Енергија коју тело прима или отпушта у топлотним процесима назива се количина топлоте – Q . Јединица за количину топлоте је џул [Ј].
Q = c·m·Δt
или
Q = c·m·ΔТ
- c – специфични топлотни капацитет је количина топлоте потребна да се један килограм супстанце загреје за један келвин, односно степен Целзијуса. Специфични топлотни капацитет зависи од врсте супстанце: ако посматрамо лонче са водом која се греје видимо да се метал пре загреје од воде. Јединица је [J/kgºC] или [J/kgK]
- m – маса, јединица [kg]
- Δt =t2-t1 или ΔТ=T2-T1 – промена температуре јединица [ºC] или [K]. Упамтите промена температуре по бројној вредности у целзијусовој скали је иста као промена температуре у келвиновој скали (нпр. нека се температура мења од 20ºC до 27ºC тада је промена температуре у целзијусовој скали Δt =t2-t1=7ºC, a у келвиновој ΔТ=T2-T1=300K-293K=7K).
Количина топлоте коју тело прима при загревању или отпушта при хлађењу зависи од масе тог тела, од специфичног топлотног капацитета супстанце и од промене температуре.
Фазни прелази
Позната су три агрегатна стања супстанце
- Чврсте имају сталан облик и запремину
- Течне имају сталну запремину, а облик им се прилагођава посуди у којој се налазе и увек имају равну површину
- Гасовите немају сталан облик ни запремину

Све супстанце се састоје из атома и молекула који се међусобно привлаче, али је та привлачна сила код неких супстанци јача, а код других слабија.
Преласци из једног у друго агрегатно стање називају се
фазни прелази.
- Ч→Т је ТОПЉЕЊЕ при загревању слабе кохезионе силе и све док се не раскину нема повећања температуре

- Т→Ч је ОЧВРШЋАВАЊЕ при хлађењу. Температура топљења је једнака температури очвршћавања.

- Т→Г је ИСПАРАВАЊЕ на температури кључања целокупна течност прелази у гас

- Г→Т је КОНДЕНЗАЦИЈА. Температура кључања је једнака температури кондензације.

- Ч→Г СУБЛИМАЦИЈА


Преношење топлоте

На различите начине:
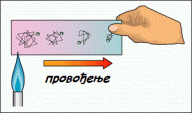
- Провођење (кондукција) – са делића на делић тела директним контактом
- Струјање (конвекција) – померају се молекули тела или нпр. загрејани слојеви ваздуха иду навише

- Зрачење (радијација) – топлотни зраци (електромагнетни зраци) преносе топлоту

Posted in
Подсетници and tagged
депозиција,
испаравање,
количина топлоте,
кондензација,
основна школа,
очвршћавање,
преношење топлоте,
седми разред,
специфични топлотни капацитет,
сублимација,
топлотно ширење тела,
топљење,
унутрашња енергија,
фазни прелази,
физика
 Отоплило је у мају, али сва срећа да се ближимо крају.
Отоплило је у мају, али сва срећа да се ближимо крају.

























